Article paru dans Recherche & Santé n°154 – La revue de la Fondation pour la Recherche Médicale – printemps 2018 /
Optimiser la survie des greffons cardiaques
L’objectif du projet INOVAGRAFT est de prolonger le temps de survie d’un cœur humain hors du corps. De quoi permettre à des greffons de voyager sur de plus grandes distances, et d’augmenter ainsi le nombre de greffes cardiaques réalisables chaque année.
Quelle est la problématique en matière de greffe cardiaque ?
Le nombre de greffes cardiaques réalisées en France est relativement stable, autour de 450 par an, alors que le nombre de personnes inscrites sur liste d’attente, lui, ne cesse d’augmenter, pour atteindre environ 1 200 actuellement.
Plusieurs pistes sont étudiées par les chercheurs pour faire face à cette pénurie de greffons : comme le développement d’un cœur artificiel, avec notamment le projet français Carmat, ou l’augmentation du nombre de donneurs greffes réalisées en permettant aux greffons de voyager en allant chercher des greffons sur de plus grandes distances. L’un des facteurs de cette pénurie est en effet la durée de survie d’un cœur hors du corps : aujourd’hui elle n’est que de 4 à 6 heures.
Quel est l’objectif du projet INOVAGRAFT ?
Un cœur prélevé en vue d’une greffe est conservé dans une boite container en plastique contenant un liquide physiologique amélioré*, elle-même placée dans de la glace. Mais même à basse température, les cellules cardiaques, qui sont de nature musculaire, supportent mal d’être privées d’oxygène.
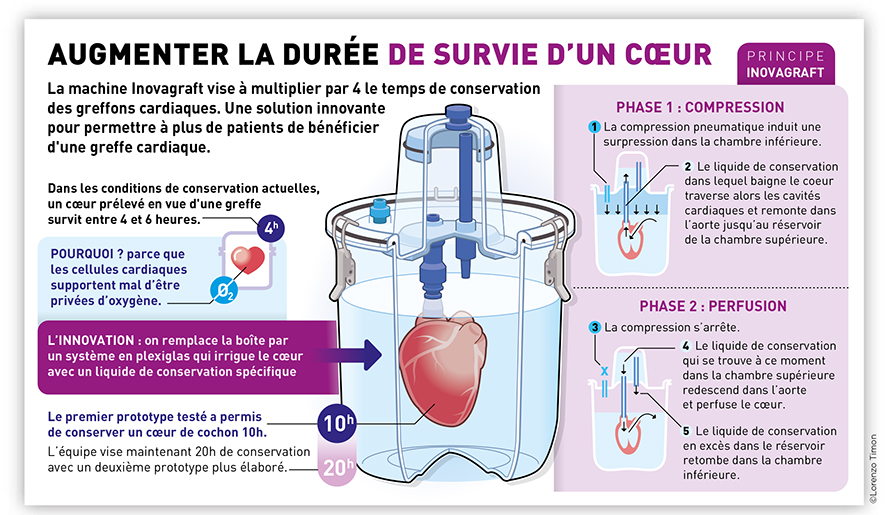
Multiplier par 4 le temps de conservation des greffons cardiaques tout en maintenant une survie optimale, et permettre ainsi de les transporter sur des plus grandes distances : tel est le but de la machine INOVAGRAFT développée par René Ferrera, ingénieur de recherche et ses collègues du Laboratoire CarMeN.
Concrètement, comment cela fonctionne ?
La boite de transport est remplacée par un système en plexiglas qui contient l’organe mais aussi le perfuse : un moteur pneumatique permet de mettre en mouvement un liquide qui rentre par l’aorte* et irrigue ainsi tout le tissu cardiaque. Il ne s’agit pas simplement de remplir oreillettes et ventricules mais bien d’atteindre les cellules cardiaques elles-mêmes pour leur apporter de quoi prolonger leur survie.
Le liquide est un mélange particulier qui contient une quinzaine de composants. Certains sont des nutriments, d’autres luttent contre d’éventuels dégâts liés à l’ischémie, notamment le risque d’œdème.
Où en est le projet actuellement ?
Un premier prototype a été testé avec des cœurs de cochons, dont la taille et les besoins métaboliques sont très proches d’un cœur humain. « Les essais ont montré qu’un cœur conservé 10 heures dans notre machine est tout à fait comparable à un cœur conservé 3 heures en simple immersion, résume René Ferrera. Nous visons maintenant 20 heures de conservation, de quoi faire voyager un cœur entre deux continents ! »
Un deuxième prototype va être construit : il renfermera notamment des capteurs permettant de mesurer en temps réel la concentration dans le liquide de certaines molécules produites par les cellules musculaires lorsqu’elles souffrent. Cette machine sera aussi « imagerie compatible » : le cœur ainsi conservé pourra passer à l’IRM, au scanner ou même à l’échographie afin que les cardiologues évaluent son état. Cela devrait permettre à des équipes de recherche d’utiliser cette machine pour évaluer l’intérêt des cœurs arrêtés* (pour l’instant non utilisés en France) afin d’élargir les possibilités de transplantation.
Quelles recherches seront menées sur le liquide de conservation ?
« Depuis que l’on greffe des organes, ceux-ci ont toujours été conservés dans de la glace, entre 0 et 4°C, car c’est simple à mettre en œuvre, rappelle René Ferrera. Mais la température idéale serrait peut-être entre 10 et 12°C. » Grâce à ce 2ème prototype qui sera doté d’un thermostat, les chercheurs comptent bien trouver la température optimale de conservation. Par ailleurs, un accord a été passé avec une entreprise de biotechnologies bretonne, Hemarina, qui travaille à la mise au point d’un sang artificiel à partir d’hémoglobine de vers marins. « L’objectif est de trouver un moyen d’apporter efficacement de l’oxygène aux cellules cardiaques pendant le transport du greffon. »
En France en 2016 :
4 748 personnes vivant avec un cœur greffé
477 greffes cardiaques réalisées
573 nouvelles personnes sur liste d’attente pour un cœur